之前從CAR-T製程過程,從細菌到病毒 (上篇)已介紹含有專一性辨認之基因片段的質體(plasmid)是如何透過細菌複製增量,接下來就是將質體送入T細胞中最終使其表現CAR於細胞表面上,送入方式常見的有電穿孔(electroporation)與病毒感染(virus infection),前者是在細胞外外加短暫高電壓,使細胞膜通透力暫時性增加來讓外源基因進入細胞中,而本篇將著重於病毒感染法來介紹。
電穿孔原理:
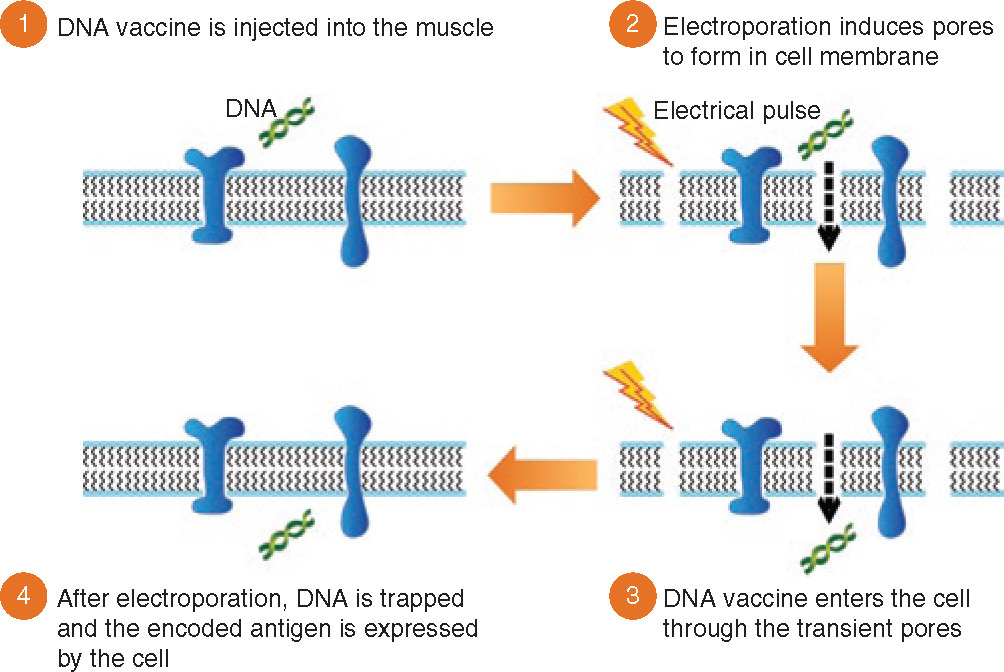
圖片來源: Mol Ther. 2009 May;17(5):922-8.
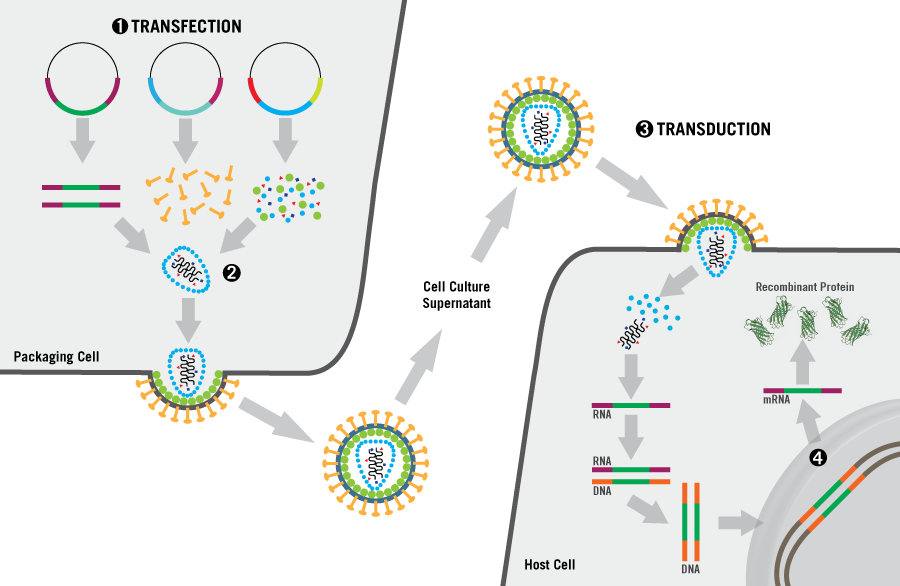
簡易的病毒感染流程如下:
何謂病毒感染式的基因轉殖呢? 簡單來說就是利用病毒會將自身DNA送到宿主細胞內的特性,將我們的目標基因送到細胞中,再利用細胞本身轉錄轉譯能力將目標基因轉譯成功能性蛋白。
在生物技術上最常使用反轉錄病毒(retrovirus)、腺病毒(adenovirus)和慢病毒(lentivirus)三種來當作我們的基因遞送者:
A: 反轉錄病毒(Retrovirus)
一種RNA病毒,進入宿主後會反轉錄作用將RNA反轉成DNA,並將DNA嵌入宿主染色體中,因此就能藉由宿主複製而複製,具外套膜且只能感染分裂中的細胞。
B: 腺病毒(Adenovirus)
為一種DNA病毒,經用內吞作用(endocytosis)進入宿主細胞中,進入後再釋出其DNA進入宿主細胞核中,不具外套膜但能感染分裂中或不分裂的細胞,腺病毒最後會破宿主細胞膜而出。
C: 慢病毒(Lentivirus)
為一種RNA病毒,屬反轉錄病毒的一種,外套膜表面與宿主細胞膜受體辨認後藉由膜融合(membrane fusion)進入宿主中,但與反轉錄病毒的差別在於其可感染分裂或不分裂的細胞。
以慢病毒為例,為降低基因轉殖操作的危險性,除了目標質體外,通常還有包裹載體(package vector,又稱結構蛋白載體 structure protein vector)及外套膜載體(envelope vector),將三者一同送入包裹細胞(packaging cell ex:293T)內進行複製、表現與病毒組裝,其經過逆轉錄作用製造載體DNA及轉譯出病毒的蛋白外殼與外套膜,最後於細胞中組裝成病毒型態後再釋放到細胞外。此過程通常需要兩到三天以蒐集足夠量且含有目標質體的病毒。
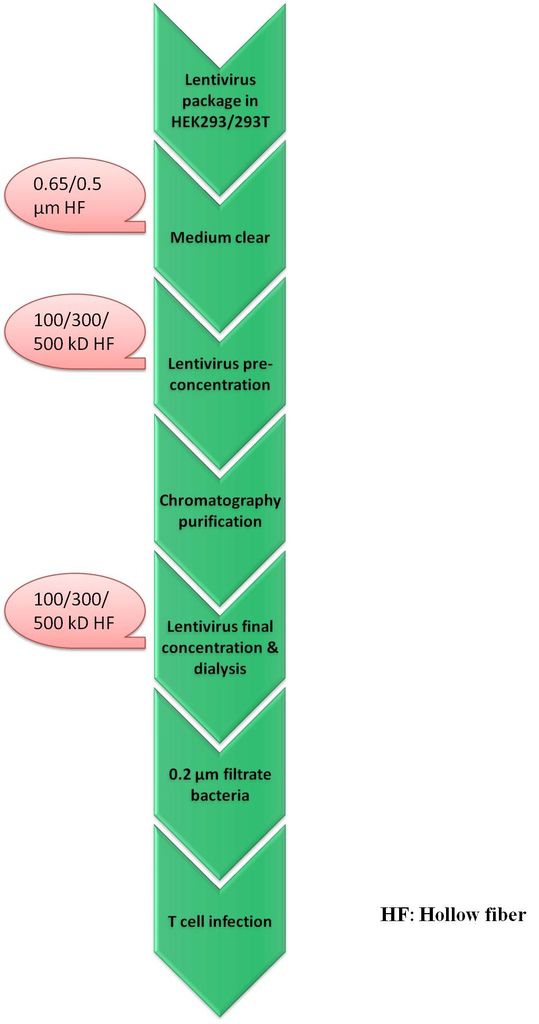
慢病毒包裝與感染步驟:
將含病毒的培養基收下來後,傳統會使用高速離心的方式分離培養基中的細胞碎屑再以超高速離心來濃縮病毒提高效價,近代則推薦使用Hollow fiber(HF) 0.5, 0.65 μm以切向流過濾的方式做培養液澄清再以300, 500 kD HF做初步濃縮,之後利用層析管柱分離出病毒,再用100, 300 kD HF做最後濃縮以及0.2 µm的無菌過濾,結合上篇所述,不論是在細菌階段或是在細胞的病毒組裝階段都可以用到切向流過濾濃縮系統(Tangential Flow system; TFF)系統來做濃縮、分離、除菌與澄清,只需更換HF與矽膠管件即可。
(參考快速病毒濃縮(無菌操作)的新思維; 不可思議!! 200倍病毒濃縮透析換液僅花35分鐘完成!!)
TFF 切向流過濾系統,從2 mL~500 L

得到濃縮後具有CAR的病毒後,接下來就可以用來感染從病患血液中分離出來的T細胞囉! 步驟如下圖:
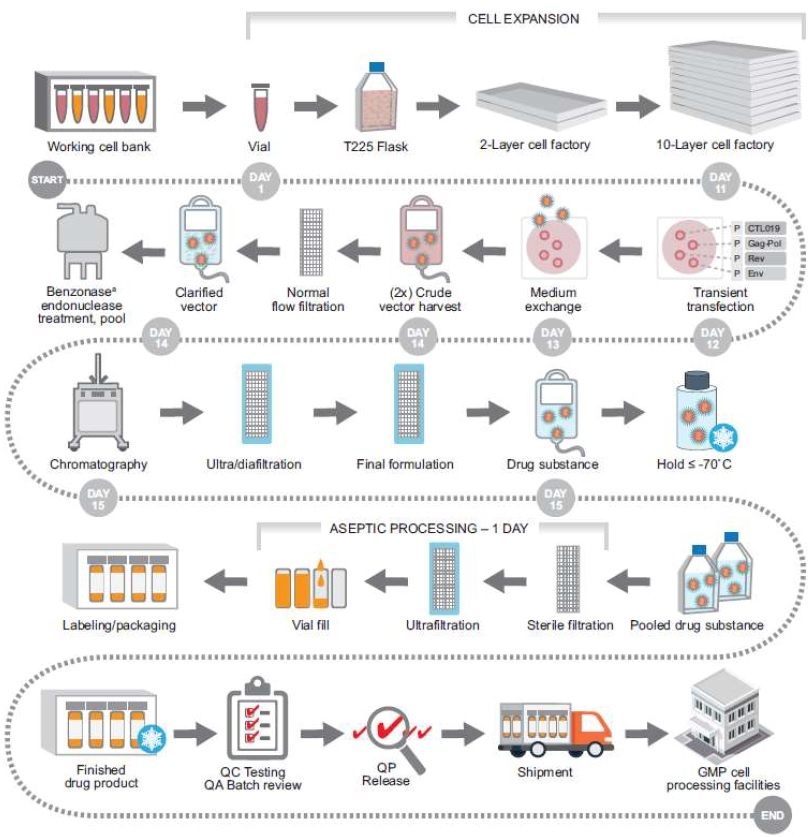
結合上下兩篇所述, 要改造T細胞的前置步驟就需經歷: 專一性質體設計、細菌轉殖培養放大、病毒包裝放大、分離濃縮等重重步驟,這樣的演進都是結合眾多科學家們辛苦研究的結晶,才造就人類在醫療技術上的突破,雖然現今CAR-T細胞治療仍有許多副作用與侷限性,不過隨著科學與醫療快速進步,期許未來CAR-T細胞療法能更廣泛的應用與更安全。
若有更多濃縮透析問題,歡迎於部落格留言與我們討論,或參考
文章標籤
全站熱搜





 留言列表
留言列表

 {{ article.title }}
{{ article.title }}